МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ТЕХНОЛОГИЧЕСКИЙ ИНСТИТУТ
ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
КАФЕДРА ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
КУРСОВАЯ РАБОТА
по дисциплине «Общая химическая технология»
на тему:
СИНТЕЗ И АНАЛИЗ ХТС В ПРОИЗВОДСТВЕ АЦЕТОНА
Выполнил:
студент группы
Проверил:
2008 г.
1. Содержание
1. Содержание 2
2. Задание
3. Введение
4. Синтез ХТС
Обоснование создания эффективной ХТС
Определение технологической топологии ХТС
Установление технологических и конструкционных
параметров ХТС, технологических параметров
режима и потоков
Химическая модель ХТС
Функциональная модель ХТС
Структурная модель ХТС
Операторная модель ХТС
Технологическая схема ХТС
5. Анализ ХТС
Представление изучаемого объекта в виде
иерархической структуры ХТС
Построение математической модели ХТС
Изучение свойств и эффективности
функционирования ХТС
6. Заключение
2. Задание
Какое количество гидроперекиси изопропилбензола необходимо, если известно, что в процессе разложения получается 6 т. толуола, степень разложения 80 %
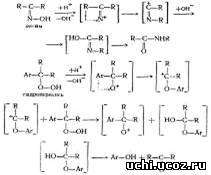
3. Введение
Ацетон СН3СОСН3 известен с 1732 г как продукт сухой перегонки солей уксусной кислоты и ранее назывался пироуксусным эфиром. Состав ацетона определили Ю. Либих и Ж. Дюма в 1832 г., а А. Уильямсон установил его строение (1852 г), которое позднее было подтверждено синтезом ацетона из цинк-диметила и хлористого ацетила.
Долгое время ацетон не имел широкого применения и производился в небольших масштабах термическим разложением уксуснокислого кальция («уксусного порошка»), получаемого при сухой перегонке древесины."
Вследствие зарождения и развития химии синтетических материалов возникла потребность в таком хорошем растворителе, каким является ацетон; это заставило искать новые способы его получения.
В настоящее время ацетон широко применяется в качестве растворителя в различных отраслях промышленности. Он является также сырьем для синтеза целого ряда соединений, в том числе растворителей более сложного строения, таких, как диа-цетоиовый спирт, окись мезитила, метилизобутилкетон, метил-изобутилкарбинол; из ацетона (через ацетонциангидрин) получают метилметакрилат, применяемый в производстве органического стекла, изофорон, уксусный ангидрид, дяфенилолпропан и другие продукты.
Разнообразие областей применения ацетона вызвало быстрый рост его производства.
В Российской Федерации ацетон применяется главным образом как растворитель в производстве автомобильных, авиационных, кабельных, кожевенных и других лаков и эмалей, кинопленок, фотореагентов, целлулоида, ацетатного шелка и т. п. Для химических синтезов используется лишь небольшая часть ацетона.
В данной работе приводится анализ различных способов получения ацетона, выбор оптимальной технологической схемы, обеспечивающей экономически эффективный, технологически целесообразный и экологически безопасный метод производства.
4. Синтез ХТС
Производство ацетона брожением крахмала
Ферментативный метод является самым старым методом получения ацетона в промышленных масштабах. В результате жизнедеятельности некоторых видов бактерий (Bacyllus acetobutylicus и др.) крахмал превращается в ацетон и n-бутиловый спирт. В качестве сырья для этого процесса чаще всего применяют кукурузную муку; из 100 кг муки можно получить 12 кг n-бутанола, 6 кг ацетона и 2 кг этилового спирта [1].
Производство ацетона из изопропилового спирта
Изопропиловый спирт в довольно больших количествах вырабатывается в различных странах путем сернокислотной или прямой гидратации пропилена. Основным потребителем изопропилового спирта является производство ацетона, который может быть получен из него двумя методами: каталитическим дегидрированием и неполным окислением (в паровой или жидкой фазе).
Каталитическое дегидрирование изопропилового спирта. Метод каталитического дегидрирования изопропилового спирта в ацетон осуществляется в промышленности США с 1923 г. и получил широкое распространение в других странах. Принципиальная схема производства ацетона этим методом показана на рис. 1. Процесс протекает в одну стадию то реакции:
СН3СН(ОН)СН3 → СН3СОСН3 + Н2 – 69,9 кДж (16,7 ккал)
В качестве катализатора Используется главным образом окись цинка, осажденная на пемзе. Повышение температуры способствует сдвигу равновесия реакции в сторону образования ацетона. По данным Кольбе и Барвелла [1], степень превращения Изопропилового спирта в ацетон при 225 °С составляет 84%, три 325 °С – 97%, при 525 °С – 100%, однако в последнем случае в значительной степени протекают побочные реакции.
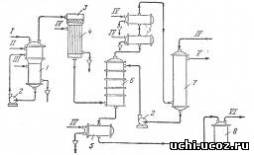
Рис. 1. Принципиальная схема производства ацетона дегидрированием изопропилового спирта:
1 – испаритель; 2 – насосы; 3 – реактор; 4 – водяной холодильник смешения; 5 – холодильники; 6 – башня снасадкой; 7 – Водяной скрубберу; 9 – сборник ацетона
I – изопропиловый спирт; II – водород; III – пар; IV – вода; V – отходящие газы; VI – товарный ацетон.
Для предотвращения образования продуктов полимеризации, отравляющих катализатор, исходный изопропиловый спирт смешивают в паровой фазе с эквимолекулярным количеством водорода. Реакцию проводят яри 380°С, степень превращения изопропилового спирта составляет 98%. Реактор представляет собой заполненный катализатором трубчатый аппарат, межтрубное пространство которого обогревается топочными газами.
После 10 суток работы требуется регенерация катализатора, так как активность его уменьшается вследствие отложения углерода на поверхности. Регенерацию осуществляют пропусканием через слой катализатора азота, содержащего – 2% кислорода, при 500 °С, Срок службы катализатора – около 6 месяцев.
Контактные газы из реактора поступают на охлаждение (при котором конденсируется около 50% ацетона), после чего их промывают водой, поглощающей ацетон. Промывные воды подвергаются фракционированию и азеотропной перегонке для выделения товарного ацетона и безводного изопропилового спирта, снова направляемого на дегидрирование.
Водород после промывки от ацетона возвращается на разбавление спирта, а водород, образовавшийся при дегидрировании, выводится из системы и используется для других синтезов. Выход ацетона составляет около 90% (считая на изопропиловый спирт). На 1 т ацетона расходуется 1,1—1,2 т изопропилового спирта или около 0,9 т пропилена [1].
Французским институтом нефти разработан способ дегидрирования изопропилового спирта в жидкой фазе. Катализатором процесса служит суспендированный в исходном спирте никель Ренея, реакцию проводят при 150 °С. В этих условиях достигаются почти количественные выходы ацетона.
Неполное окисление изопропилового спирта в паровой фазе.
Реакция неполного окисления изопропилового спирта
СН3СН(ОН)СН3 + 0,5 О2 → СН3СОСН3 + Н3О + 180 кДж (43 ккал)
протекает в присутствии металлических катализаторов – меди, серебра, никеля, платины и т. д.
Высокий выход ацетона достигается при использовании серебра, осажденного на пемзе, или серебряной сетки. Температура реакции может изменяться в широких пределах (450— 650 °С) и выбирается в зависимости от применяемого катализатора, объемной скорости паров спирта и воздуха и других факторов.
Перед подачей реагентов в контактный аппарат (рис. 2) изопропиловый спирт испаряют в испарителе-сатураторе, насыщают парами воздуха и перегревают полученную паровоздушную смесь. Реакция протекает в адиабатических условиях, т. е. тепло, выделяющееся в процессе окисления, воспринимается самой реакционной смесью.
При окислении, «роме ацетона, образуется также некоторое количество побочных продуктов, в том числе уксусной кислоты и ацетальдегида. Поэтому контактные газы после прохождения ими металлического катализатора пропускают через насадку в виде слоя мела, на которой уксусная кислота и ацетальдегид почти количественно превращаются в ацетон. Оптимальной для этой реакции является температура 450 °С, достигаемая охлаждением контактных газов во встроенном в реактор змеевике.
Из контактного аппарата газы поступают в котел-утилизатор, а затем последовательно на «парциальную» конденсацию и водную абсорбцию. Несконденсировавшиеся газы после абсорбции ацетона водой сбрасывают в атмосферу. Промывные воды из скруббера объединяют с конденсатом и направляют на ректификацию.
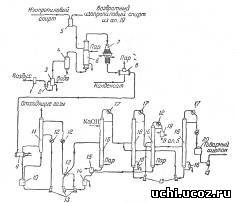
Рис. 2. Принципиальная схема производства ацетона неполным окислением изопропилового спирта в паровой фазе:
1 – висциновый фильтр; 2 – ротационный компрессор; 3, 9, 12, 19 – холодильники; 4 – ресивер; 5 – сборник изопропилового спирта; 6 – испаритель-сатуратор; 7 – контактный аппарат; 8 – котел-утилизатор; 9 – сборник конденсата; 10 – скруббер; 11 – насосы; 12 – сборник сточной воды; 15 – сепаратор; 16 – ректификационные колонны; 17 – дефлегматоры; 18 – кипятильники; 20 – сборник ацетона.
В первой по ходу процесса ректификационной колонне из водного раствора отгоняют ацетон и изопропиловый спирт. В верхнюю часть колонны для очистки от осмоляющихся примесей подают 15%-ный раствор NaOH. Вода из куба колонны после осаждения органических веществ и утилизации ее тепла подается в скруббер на абсорбцию ацетона.
В следующей колонне происходит разделение продуктов на ацетон-сырец и раствор изопропилового спирта. Ацетон-сырец поступает на ректификацию для выделения товарного ацетона; изопропиловый спирт выделяют перегонкой из водного раствора и возвращают на окисление.
Неполное окисление изопропилового спирта в жидкой фазе.
Интересным методом получения ацетона из изопропилового спирта является его неполное окисление и жидкой фазе. Этот метод, применяемый для производства перекиси водорода, осуществляется с 1957 г. на заводе фирмы «Shell Chemical Со.» в США [2].
Процесс протекает по схеме
СН3СН(ОН)СН3 + О2 → СН3СОСН3 + Н2О2
и проводится автокаталитически при 90 – 140°С под давлением, позволяющем удерживать смесь в жидкой фазе. В качестве окислителя можно применять как воздух, так и кислород.
Реактор должен быть изготовлен из материалов, не разлагающих перекись водорода. На окисление подают 89%-ный раствор изопропилового спирта; по достижении концентрации перекиси водорода 15 – 25% продукт выводится из реактора, разбавляется водой и стабилизируется. Ацетон и не прореагировавший спирт отгоняют и очищают, перекись водорода концентрируют быстрым испарением и вакуум-перегонкой.
Выход ацетона составляет 95% от теоретического, выход перекиси водорода – около 87 %25.
Другие методы получения ацетона
Ацетон получается также в качестве побочного продукта в синтезе аллилового спирта из изопропилового спирта и акролеина:
СН3–СН(ОН) –СН3 + СН2=СН–СНО → СH2=СН–СН2ОН + СН3–СО–СН3
Эта реакция проводится в паровой фазе при 350–450 °С и атмосферном давлении в присутствии катализатора – смеси окиси магния и окиси цинка.
Данный процесс, так же как и процесс получения ацетона и перекиси водорода из изопропилового спирта, является составной частью синтеза глицерина по методу американской фирмы «Shell Chemical Со.»:
а) пропилен → изопропиловый спирт → ацетон + перекись водорода
б) пропилен → акролеин
в) акролеин + изопропиловый спирт → аллиловый спирт + ацетон
г)