Решебник
разноуровневых заданий
по химии
для дифференцированного контроля
знаний учеников
8 класс
г. Кривой Рог
2001 год
Вариант 1
Задачи
Первый уровень
1.
| Дано: О2 | 1. Определяем относительную плотность 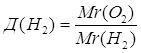  |
| Д(Н2) — ? |
| Ответ: | относительная плотность кислорода по водороду 16. |
| | |
2.
| Дано: Н2О | 1. Определяем массовую долю оксигена в воде 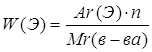  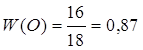 или 87% или 87% |
| W(O) — ? |
| Ответ: | массовая доля оксигена в воде 87%. |
| | |
3. О2 – молекула простого вещества – кислорода, состоящая из двух атомов оксигена.
2О2 – две молекулы простого вещества, каждая из которых состоит из двух атомов оксигена.
О – один атом оксигена.
10Н2О – десять молекул сложного вещества, каждая из которых состоит из двух атомов гидрогена и одного атома оксигена.
4СО2 – четыре молекулы сложного вещества, каждая из которых состоит из одного атома карбона и двух атомов оксигена.
4. HNO3
Второй уровень
5.
| Дано: ν(N2)=5 моль | $IMAGE6$ 1. Определяем число молекул азота $IMAGE7$ $IMAGE8$ 2. Определяем число атомов нитрогена $IMAGE9$ |
| N(N2) — ? N(N) — ? |
| Ответ: | в 5 моль азота содержится 30∙1023 молекул азота и 60∙1023 атомов нитрогена. |
| | |
6.
| Дано: m(Cu)=16 кг | х 16кг CuO + H2 = Cu + H2O 1 кмоль 1 кмоль 80кг/моль 64кг/моль 80кг 64кг 1. Определяем массу купрум (II) оксида х:80кг=16кг:64кг $IMAGE10$ | |
|
| m(CuO) — ? | |
| Ответ: | для получения 16кг меди надо взять 20кг купрум (II) оксида. | |
| | | |
7.
| Дано: V(H2)=16л | 2H2+O2=2H2O 1. Определяем объем кислорода V(H2):V(O2)=2:1=16л:х $IMAGE11$ |
| V(O2) — ? |
| Ответ: | на полное сгорание 16 литров водорода пойдет 8л кислорода. |
| | |
Третий уровень
8. 2Ca+O2=2CaO
CaO+H2O=Ca(OH)2
Ca(OH)2+2HCl=CaCl2+2H2O
9.
| Дано: Д(О2)=1,5 | 1. Определяем относительную молекулярную массу озона $IMAGE12$ Mr(озона)=Д(О2)∙Mr(O2) Mr(озона)=1,5∙32=48 2. Определяем формулу озона 16 – 1 атом 48 – х атомов $IMAGE13$ |
| Формула озона — ? |
| Ответ: | формула озона – О3. |
| | |
10. При увеличении давления химическое равновесие сместится в сторону образования водорода и кислорода.
Вариант 2
Задачи
Первый уровень
1.
| Дано: CaCO3 | $IMAGE14$ 1. Определяем массовую долю кальция $IMAGE15$ или 40% |
| W(Ca) — ? |
| Ответ: | массовая доля кальция в кальций карбонате 40%. |
| | |
2.
| Дано: N(H2)=24∙1023 молекул | 1. Определяем количество вещества водорода $IMAGE16$ $IMAGE17$ |
| ν(H2) — ? |
| Ответ: | количество вещества водорода – 4моль. |
| | |
3.
| Дано: Д(Н2)=8 | 1. Определяем Mr(в-ва) $IMAGE18$ Mr(в-ва)=Д(Н2)∙Mr(H2) Mr(в-ва)=8∙2=16 |
| Mr(в-ва) — ? |
| Ответ: | относительная молекулярная масса вещества – 16. |
| | |
4 2Br – два атома брома
Br – один атом брома
3HBr – три молекулы сложного вещества, каждая из которых
Второй уровень
5.
| Дано: ν(AgNO3)=3моль | 3моль хг AgNO3 + NaCl = AgCl + NaNO3 1моль 1моль 143,5г/моль 143,5г 1. Определяем массу аргентум хлорида 3моль:1моль=х:143,5г $IMAGE19$ |
| m(AgCl) — ? |
| Ответ: | масса аргентум хлорида 430,5г. |
| | |
6.
| Дано: S V(O2)=44,8л | 44,8л х S + O2 = SO2 1моль 1моль 22,4л/моль 22,4л/моль 22,4л 22,4л 1. Определяем объем сульфур (IV) оксида 44,8л:22,4л=х:22,4л $IMAGE20$ |
| V(SO2) — ? |
| Ответ: | объем сульфур (IV) оксида – 44,8л. |
| | |
7. С повышением температуры химическое равновесие сместится в сторону исходных веществ.
Третий уровень
8. 2Pb+O2=2PbO
PbO+2HCl=PbCl2+H2O
PbCl2+2AgNO3=Pb(NO3)2+2AgCl↓
9. а) CuO+2HNO3=Cu(NO3)2+H2O
10.
| Дано: m(H2SO4)=4,9г NaOH | 4,9г хг 2NaOH + H2SO4 = Na2SO4 + 2H2O 1моль 1моль 98г/моль 142г/моль 98г 142г 1. Определяем массу натрий сульфата 4,9г:98г=х:142г $IMAGE21$ |
| m(Na2SO4) — ? |
| Ответ: | в результате взаимодействия 4,9г сульфатной кислоты с натрий гидроксидом образуется 7,1г натрий сульфата. |
| | |
Вариант 3
Задачи
Первый уровень
1.