Контрольная работа
по химии
вариант № 2
2009
Контроль за процессами ассоциации и связывания противоионов методом ЯМР
Полная характеристика самоассоциации молекул ПАВ должна включать зависимости концентраций всех частиц от общей концентрации ПАВ. Поскольку невозможно измерить концентрации всех мицелл с разными числами агрегации, прибегают к оценке некоторых подходящих средних величин. Зададим концентрации молекулярно растворенного и находящегося в мицеллах ПАВ, а также концентрации связанных и свободных противоионов и гидратацию мицелл. С помощью ПАВ - и противоионоселективных электродов можно оценить активности ПАВ и противоионов, что дает информацию о распределении между мицеллярным и несвязанным состояниями. Еще более полную информацию можно получить при измерении коэффициентов самодиффузии молекул ПАВ, мицелл ПАВ, противоионов и молекул воды. В настоящее время такую информацию можно получить в одном быстром эксперименте с использованием метода ЯМР. В качестве поясняющего примера на рис. приведены результаты измерений для дихлорацетата дециламмония. KKM этого ПАВ составляет 26 мм.
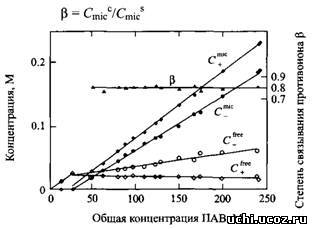
Коэффициенты самодиффузии представляют собой средневзвешенные величины по различным окружениям, поэтому
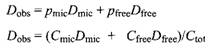
Зависимости коэффициентов самодиффузии ионов поверхностно-активного вещества, противоионов, молекул воды и мицелл от общей концентрации поверхностно-активного вещества в системе, где с, DnC соответственно обозначают долю молекул в определенном окружении, коэффициент самодиффузии и концентрацию.
Значение Dfree определяют из измерений при С меньших ККМ, a Amc - для образцов, в которых молекулы заключены в мицеллы. В исследованиях, результаты которых представлены на рис., чтобы избежать влияния на процесс мицеллообразования, использованы низкие концентрации плохо растворимого тетраметилсилана. Поскольку мицеллы представляют собой довольно большие образования, значения их коэффициентов самодиффузии гораздо меньше соответствующих величин для молекулярно растворенных ПАВ.
Как видно из рис., коэффициенты самодиффузии различных молекул сильно отличаются друг от друга при концентрациях ПАВ, значительно превышающих ККМ. Молекулы воды менее всего ассоциированы с мицеллами, тогда как молекулы TMC локализованы в мицеллах в гораздо большей степени. Результаты количественного анализа, вытекающие из измерений диффузии ПАВ и противоионов, представлены на рис.
Отметим некоторые важные закономерности, характерные для мицеллообразования ионных ПАВ.
1. С хорошим приближением можно считать, что все молекулы ПАВ ниже KKM находятся в молекулярно растворенном состоянии.
2. При концентрациях выше KKM концентрация молекулярно растворенного ПАВ уменьшается и может достигать значений, существенно меньших ККМ.
3. Концентрация свободных противоионов увеличивается с ростом суммарной концентрации ПАВ сильнее при концентрациях ниже ККМ, чем при концентрациях выше ККМ.
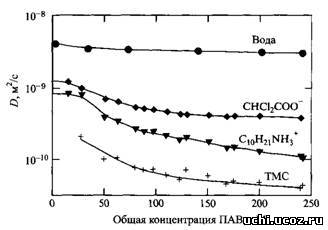
4. Соотношение концентраций связанных с мицеллами противоионов и ПАВ в мицелле определяет степень связывания противоинов:
Зависимости концентраций мицелл и свободных ионов ПАВ и противоионов от суммарной концентрации ПАВ, в - степень связывания противоионов.
Очень важно, что в остается постоянной величиной при увеличении мицеллярной концентрации на порядки. Обычно это объясняют конденсацией противоионов на мицелле. Это означает, что ассоциация противоионов с мицеллой растет до определенного уровня, обеспечивающего некоторую эффективную плотность заряда мицеллы, а затем остается практически постоянной. В этих условиях ассоциация противоионов с мицеллой не зависит от концентрации мицелл, а также концентрации вводимого электролита и от температуры. Явление конденсации противоионов характерно для любых систем с высокой плотностью заряда, включая полиэлектролиты и заряженные поверхности, что хорошо объясняется с позиций электростатической теории.
Солюбилизация гидрофобных веществ в мицеллах
Тетраметилсилан представляет пример вещества, солюбилизируемого мицеллами, т.е. вещества, которое становится растворимым в водной фазе в присутствии мицелл. Обычно растворимость солюбилизата остается очень низкой до KKM и быстро увеличивается после достижения KKM и практически всегда линейно с увеличением концентрации ПАВ.
Солюбилизация - это очень важное явление, характерное для растворов ПАВ. Оно к тому же имеет прямое отношение к моющему действию и составлению композиций фармацевтических препаратов. Это явление будет неоднократно обсуждаться по ходу изложения материала в данной книге, например при рассмотрении фазовых диаграмм, дающих количественную информацию о способности мицелл включать в свой состав различные молекулы. Для изучения солюбилизационных равновесий и описания термодинамики солюбилизации в наибольшей мере подходит упомянутый выше метод измерения коэффициентов самодиффузии.

Зависимость солюбилизации красителя от концентрации растворов алканоатов калия
Ход изотерм поверхностного натяжения растворов ПАВ, содержащих примеси, объясняется явлением солюбилизации. Например, при измерении поверхностного натяжения растворов додецилсульфата натрия часто обнаруживается минимум, который устраняется после очистки ПАВ. Оказалось, что ДСН, как правило, загрязнен додеканолом. Додеканол характеризуется большей поверхностной активностью, чем ДСН, и поэтому легче концентрируется на поверхности вода - воздух. Но как только начинают образовываться мицеллы, появляется другое, более энергетически выгодное место локализации спирта - в мицеллах. Додеканол удаляется с поверхности в результате солюбилизации, и поэтому поверхностное натяжение раствора увеличивается.
Размер и структура мицелл
В широкой области концентраций выше KKM мицеллы можно представить как микроскопические капли углеводорода, окруженные полярными группами, взаимодействующими с водой. Радиус мицеллярного ядра, состоящего из алкильных цепей, близок к размеру вытянутой алкильной цепи, т.е. - 1.5-3.0 нм. Почему это так?
Движущей силой мицеллообразования является устранение контакта между алкильными цепями и водой. Чем крупнее сферическая мицелла, тем более эффективно это устранение, поскольку увеличивается отношение объема мицеллы к ее поверхности. Уменьшение радиуса мицеллы всегда сопряжено с увеличением контакта углеводород-вода. В то же время если сферическая мицелла становится настолько большой, что молекула ПАВ оказывается меньше расстояния от поверхности мицеллы до ее центра, то в мицелле возникают пустоты либо некоторая часть молекул теряет контакт с поверхностью, перенося таким образом полярные группы в центр мицеллы. И то и другое энергетически невыгодно.
Тот факт, что радиус мицеллы примерно равен длине вытянутой молекулы ПАВ, вовсе не означает, что все молекулы ПАВ в мицелле вытянуты. Достаточно, чтобы хотя бы одна молекула была вытянутой, чтобы выполнялись указанные требования. Основная доля молекул ПАВ находятся в мицелле в разупорядоченном состоянии с большим вкладом гошконформаций. Детали состояния алкильных цепей в мицелле исследуются спектроскопическими методами. Установлено, что это состояние близко к состоянию в жидком алкане. Жидкоподобное состояние отчетливо проявляется также в молекулярной динамике. Так, изомеризация цепей происходит за несколько десятков пикосекунд, что лишь немного медленнее, чем для жидких алканов. Из-за ограничений, обусловленных закреплением на поверхности мицеллы, движение становится слабо анизотропным.
Капельная модель объясняет солюбилизирующую способность мицелл по отношению к широкому кругу неполярных и слабополярных веществ. В то же время локализация солюбилизата в мицелле сильно зависит от его природы. Молекулы насыщенного углеводорода равномерно распределяются внутри мицеллярного ядра, а молекулы ароматических веществ, в силу их некоторой поверхностной активности, как и длинноцепочечные спирты, преимущественно локализуются в поверхностной части мицеллы и ориентируются так же, как молекулы ПАВ, образующие мицеллу. На поверхности мицеллы находятся ассоциированные с ней противоионы в количестве 50-80% от ионов ПАВ и их количество мало зависит от условий. Простые неорганические противоионы очень слабо ассоциируются с мицеллой. Из-за их мобильности специфический комплекс с определенным расстоянием между полярной группой и противоионом не образуется. Противоины ассоциируются с мицеллой за счет дальнодействующих электростатических сил. Противоионы остаются в значительной степени гидратированными, особенно сильно склонность к сохранению гидратных оболочек выражена у катионов. Некоторая доля гидратационной воды обеспечивается ассоциированными противоионами; кроме того, полярные группы всегда сильно гидратированы. В то же время молекулы воды эффективно исключаются из мицеллярного ядра. Вследствие геометрических ограничений некоторая часть углеводородных цепей неизбежно будет находиться на поверхности мицеллы, но даже на небольшом расстоянии от этой поверхности вероятность нахождения молекул воды ничтожно мала. Размер мицелл, выраженный как радиус сферического агрегата, оценивают также с помощью методов светорассеяния и измерений коэффициентов самодиффузии. Не менее важной характеристикой мицеллы является мицеллярное число агрегации. Для его определения лучше всего подходит метод тушения флуоресценции. Например, число агрегации ДСН в мицеллах при 25 0C составляет 60-70. Число агрегации надежно определяется только для достаточно узкого распределения. Мицеллы с разными числами агрегации сосуществуют в равновесии друг с другом, но вероятность заметного отклонения числа агрегации от среднего значения чрезвычайно мала.
По этой причине модель, основанная на законе действующих масс, хорошо описывает мицеллярную систему.
Для этой модели с учетом основного соотношения между свободной энергией и константой равновесия К.

можно вывести приближенное выражение для мицеллообразования:
$IMAGE6$
где AG0 - разность стандартной свободной энергии молекулы в мицелле и в некотором выбранном стандартном состоянии сравнения, что служит стартовой точкой для термодинамического описания мицеллообразования.
Геометрические принципы упаковки цепей
Число агрегации может быть выражено как отношение объема ядра мицеллы Fmic к объему одной цепи н:
$IMAGE7$
где Rmk - радиус мицеллы. Число агрегации можно выразить и другим способом - как отношение мицеллярной площади Ат\с к площади поперечного сечения а одной молекулы ПАВ:
$IMAGE8$
Приравнивая эти два выражения, получим:
$IMAGE9$
Учитывая, что радиус мицеллы Rm\c не может быть больше длины вытянутой алкильной цепи молекулы ПАВ, равной Zmax, для сферической мицеллы находим:
$IMAGE10$ и
$IMAGE11$
Отношение v/ является геометрической характеристикой молекулы ПАВ; этот параметр чрезвычайно полезен при обсуждении типа структуры, которую образует данное дифильное вещество; он называется критическим параметром упаковки или числом ПАВ.
Кинетика мицеллообразования мицеллы образуются в ступенчатых процессах, поэтому элементарную стадию мицеллообразования можно представить как равновесие между молекулой и мицеллярным агрегатом
$IMAGE12$
где константа скорости прямой реакции лимитируется диффузией и практически не зависит ни от размера молекул ПАВ, ни от размера мицеллы.
Константа скорости обратного процесса L·, наоборот, сильно зависит от длины алкильной цепи, размера мицеллы и т.д. Вследствие кооперативности мицеллообразования на кривой распределения по размерам имеется глубокий минимум. В результате восстановление равновесия после отклонения от него осуществляется в два этапа. В быстром процессе достигается квазиравновесие при ограничении постоянного общего числа мицелл. В быстром процессе происходит перераспределение молекул ПАВ между имеющимися мицеллами. Для достижения истинного равновесия число мицелл должно изменяться. Вследствие ступенчатости процесса в него вовлекаются также промежуточные мицеллы, концентрация которых очень мала, поэтому данный процесс - медленный.
Из кинетических измерений быстрого процесса определяются два времени релаксации, характеризующие молекулярные процессы в мицеллярных растворах: фй характеризует скорость, с которой молекулы ПАВ обмениваются между мицеллами, в то время как Т2 характеризует скорость, с которой мицеллы образуются и распадаются. Примеры времен релаксации приведены в табл.2.6 Заметим, что фй имеет порядок 10 мкс для додецилсульфата натрия, а Т2 - больше миллисекунды. Оба релаксационных процесса заметно замедляются при возрастании длины алкильной цепи молекул ПАВ.
Поскольку медленный релаксационный процесс определяется распределением мицелл по размерам, кинетические измерения можно использовать для определения стандартного отклонения распределения. Распределение по размерам становится относительно узким с увеличением длины алкильной цепи.
Кинетические параметры ассоциации алкилсульфатов в мицеллы и диссоциации их мицелл:
$IMAGE13$
Времена релаксации ф й и ф2 для некоторых алкил сульфатов натрия
$IMAGE14$
Агрегирование поверхностно-активных веществ в неводных средах
Полярные растворители
В сильнополярных растворителях мицеллообразование ка