Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
«ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Электротехнический институт
Направление 551300–Электротехника, электромеханика и электротехнологии
Кафедра – Электропривода и электрооборудования
Реферат по дисциплине
«Источники гарантированного и бесперебойного электропитания промышленных предприятий»
на тему НИКЕЛЬ-МЕТАЛЛОГИДРИДНЫЕ АККУМУЛЯТОРЫ
Студенты группы 7М142
Крупина Н.В._______________
Кондрашов С.А._____________
«_____»________________
Руководитель профессор, д.т.н.
Гарганеев А.Г._______________
«_____»___________2009г.
Томск – 2009
Содержание
Введение
1. Терминология
2. Аккумуляторы: виды и происхождение
3. Никель-металлогидридные аккумуляторы
4. Основные процессы Ni-MH аккумуляторов
5. Конструкция электродов Ni-MH аккумуляторов
6. Конструкция Ni-MH аккумуляторов
7. Характеристики Ni-MH аккумуляторов
8. Зарядка Ni-MH аккумулятора
9. Достоинства и недостатки Ni-MH аккумуляторов
10. Стандарты и обозначения НМ-аккумуляторов
11. Хранение и эксплуатация Ni-MH аккумуляторов
12. Производители и перспективность НМ-аккумуляторов
13. Утилизация
Заключение
Список использованных источников
Введение
Практически невозможно представить современный мир без всякого рода электронной техники. Цифровые технологии настолько удачно вписались в нашу жизнь, сделав ее удобней и интересней, что отказаться от них мы уже просто не в силах.
Однако не стоит забывать, что для работы мобильных устройств нужны портативные источники питания, которые смогли бы обеспечить все более возрастающие потребности современной электроники. Мы получили WiFi и Bluetooth, освободившись от проводов для передачи данных, но мы все еще остаемся привязанными к электрическим сетям.
Прикладная наука, однако, не стоит на месте, предлагая все новые и новые виды источников электроэнергии. С другой стороны все же странно, что при наличии такого числа новых технологий, у нас все еще «умирают» батарейки телефонов, смартфонов, КПК и прочих гаджетов. Происходит это потому, что люди задумываются над правильным обращением с аккумулятором исключительно тогда, когда он окончательно вышел из строя и его со спокойной душой можно сдать в утиль. При этом следует понимать, что замена аккумулятора может влететь в копеечку. Не спорим, мало кому нравится строго соблюдать правила эксплуатации, но, к сожалению, только таким образом долговечность аккумулятора может быть доведена до максимума.
На сегодняшний день распространены аккумуляторы пяти различных электрохимических схем никель-кадмиевые (Ni-Cd), никель-металлогидридные (Ni-MH), свинцово-кислотные (Sealed Lead Acid, SLA), литий-ионные (Li-Ion) и литий-полимерные (Li-Polymer). Определяющим фактором для всех перечисленных элементов питания является не только портативность (т.е. небольшой объем и вес), но и высокая надежность, а также большое время работы. Основные параметры аккумулятора - это энергетическая плотность (или удельная энергия по массе), число циклов заряд/разряд, скорости зарядки и саморазряда. Cвинцово-кислотный аккумулятор состоит, как правило, из двух пластин (электродов), помещенных в электролит (водный раствор серной кислоты). У никелево-кадмиевого элемента отрицательные и положительные пластины скатаны вместе и помещены в металлический цилиндр. Положительная пластина состоит из гидроксида никеля, а отрицательная - из гидроксида кадмия. Две пластины изолированы разделителем, который увлажнен электролитом.
Никелево-металлогидридный аккумулятор конструктивно похож на никелево-кадмиевый аккумулятор, но имеет иной химический состав электролита и электродов. В литиево-ионном аккумуляторе электроды и сепаратор (разделитель) помещены в электролит из литиевой соли.
Существует огромное количество мифов и легенд о якобы идеальном режиме эксплуатации, о способах «тренировки», хранения, методах и режимах зарядки и восстановления аккумуляторов, но давайте попробуем разобраться.
1.Терминология
Аккумулятор (от лат. аccumulator — собиратель, accumulo — собираю, накопляю) — устройство для накопления энергии с целью ее последующего использования. Электрический аккумулятор преобразует электрическую энергию в химическую и по мере надобности обеспечивает обратное преобразование. Зарядка аккумулятора происходит путем пропускания через него электрического тока. В результате вызванных химических реакций один из электродов приобретает положительный заряд, а другой — отрицательный.
Аккумулятор, как электрический прибор, характеризуется следующими основными параметрами: электрохимической системой, напряжением, электрической емкостью, внутренним сопротивлением, током саморазряда и сроком службы.
Емкость аккумулятора — количество энергии, которой должен обладать полностью заряженный аккумулятор. В практических расчетах емкость принято выражать ампер-часах (  ). Количество ампер-часов показывает период времени, в течение которого будет работать данный аккумулятор при силе тока в 1 ампер. Стоит, правда, добавить, что в современных мобильных устройствах используются токи гораздо меньшей силы, поэтому емкость аккумуляторов часто измеряется в милиампер-часах (
). Количество ампер-часов показывает период времени, в течение которого будет работать данный аккумулятор при силе тока в 1 ампер. Стоит, правда, добавить, что в современных мобильных устройствах используются токи гораздо меньшей силы, поэтому емкость аккумуляторов часто измеряется в милиампер-часах ( 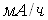 или
или  , или mAh). Номинальная емкость (как должно быть) всегда указывается на самом аккумуляторе или на его упаковке. Однако реальная емкость не всегда совпадает с номинальной. На практике, реальная емкость аккумулятора колеблется в пределах от 80% до 110% от номинального значения.
, или mAh). Номинальная емкость (как должно быть) всегда указывается на самом аккумуляторе или на его упаковке. Однако реальная емкость не всегда совпадает с номинальной. На практике, реальная емкость аккумулятора колеблется в пределах от 80% до 110% от номинального значения.
Удельная емкость — отношение емкости аккумулятора к его габаритам или массе.
Цикл — одна последовательность заряда и разряда аккумулятора.
Эффект памяти — потеря емкости аккумулятора в процессе его эксплуатации. Она проявляется в тенденции аккумулятора приспосабливаться к рабочему циклу, по которому батарея работала определенный период времени. Другими словами, если заряжать аккумулятор несколько раз, не разрядив его перед этим полностью, он как бы «запоминает» свое состояние и в следующий раз просто не сможет разрядиться полностью, следовательно, емкость его уменьшается. По мере увеличения числа зарядно-разрядных циклов эффект памяти проявляется все отчетливее.
При таких условиях эксплуатации внутри аккумулятора происходит увеличение кристаллов на пластине (о строении аккумуляторов будет рассказано ниже), которые и уменьшают поверхность электрода. При мелких кристаллических образованиях внутреннего рабочего вещества площадь поверхности кристаллов максимальна, следовательно, максимально и количество энергии, запасаемой аккумулятором. При укрупнении кристаллических образований в процессе эксплуатации — площадь поверхности электрода уменьшается и, как следствие, уменьшается реальная емкость.
На рисунке 1 изображено действие эффекта памяти.
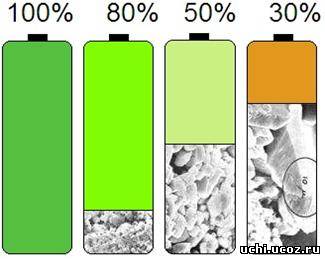
Рисунок 1 – Эффект памяти.
Саморазряд — самопроизвольная потеря аккумулятором запасенной энергии с течением времени. Это явление вызвано окислительно-восстановительными процессами, протекающими самопроизвольно, и присуще всем типам аккумуляторов, независимо от их электрохимической системы. Для количественной оценки саморазряда используется величина потерянной аккумулятором за определенное время энергии, выраженная в процентах от значения, полученного сразу после заряда. Саморазряд максимален в первые 24 часа после заряда, поэтому оценивается как за первые сутки, так и за первый месяц после заряда. Величина саморазряда аккумулятора в значительной степени зависит от температуры окружающей среды. Так, при повышении температуры выше 100°С саморазряд может увеличиться в два раза.
2. Аккумуляторы: виды и происхождение
Лидирующее положение на рынке по производству аккумуляторов занимает Япония, Тайвань, Китай, Южная Корея, и они постоянно увеличивают масштабы своего «скромного» присутствия на мировом рынке.
На рынке сегодня присутствуют десятки различных конструкций аккумуляторов, и каждая фирма-изготовитель старается достичь оптимального сочетания характеристик — высокой емкости, малых размеров и веса, работоспособности в широком температурном диапазоне и в экстремальных условиях.
В то же время исследования показывают, что более 65% пользователей мобильной и портативной техники хотят иметь еще более емкие аккумуляторы, и они готовы заплатить немалые деньги за возможность пользоваться «машинкой» (или телефоном) в течение нескольких дней без подзарядки. Именно поэтому в большинстве случаев, требуется покупка более емкой батареи, чем идущая в комплекте.
По электрохимической системе аккумуляторы делятся на несколько видов:
- свинцово-кислотные (Sealed Lead Acid, SLA);
- никель-кадмиевые (Ni-Cd);
- никель-металлогидридные (Ni-MH);
- литий-ионные (Li-Ion);
- литий-полимерные (Li-Pol);
- топливные.
В современной портативной электронике свинцовые аккумуляторы уже не используются, поэтому мы начнем наш экскурс с никелевых батарей, все еще применяемых в аккумуляторах для фотоаппаратов, ноутбуков, видеокамер и других устройств.
Родоначальником никелевых аккумуляторов были никель-кадмиевые (Ni-Cd) батареи, изобретенные еще в далеком 1899 году шведским ученым Вальдемаром Юнгнером (Waldmar Jungner). Принцип их работы заключался в том, что никель выступает в качестве положительного электрода (катода), а кадмий в качестве отрицательного (анода). На первых порах это был открытый аккумулятор, в котором кислород, выделяющийся во время заряда, уходил прямиком в атмосферу, что мешало созданию герметичного корпуса и, вкупе с дороговизной необходимых материалов, заметно притормозило начало массового производства.
C 1932 года предпринимались попытки возобновить эксперименты. В то время была предложена идея введения внутрь пористого пластинчатого никелевого электрода из активных металлов, которые обеспечили бы лучшее движение зарядов и значительно снизили бы стоимость производства аккумуляторов.
Но только после второй мировой войны (в 1947 году) разработчики пришли к почти современной схеме герметичных Ni-Cd аккумуляторов. При такой конструкции внутренние газы, выделяющиеся во время заряда поглощались не прореагировавшей частью катода, а не выпускались наружу, как в предыдущих вариантах.
Если по каким-либо причинам (превышение зарядного тока, понижение температуры) скорость анодного образования кислорода окажется выше скорости его катодной ионизации, то резкое повышение внутреннего давления может привести к взрыву аккумулятора. Для предотвращения этого корпус батареи изготавливается из стали, а иногда даже имеется предохранительный клапан.
С тех пор конструкция Ni-Cd батарей существенных изменений не претерпела (рисунок 2).
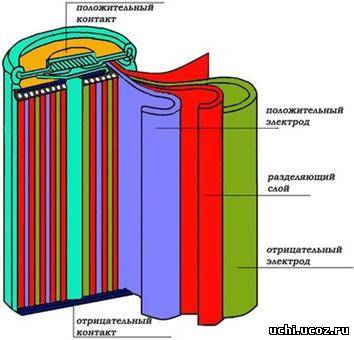
Рисунок 2 - Строение Ni-Cd аккумулятора
Основу любого аккумулятора составляют положительный и отрицательный электроды. В данной схеме положительный электрод (катод) содержит гидрооксид никеля NiOOH с графитовым порошком (5-8%), а отрицательный (анод) — металлический кадмий Cd в виде порошка.
Аккумуляторы этого типа часто называют рулонными, так как электроды скатаны в цилиндр (рулон) вместе с разделяющим слоем, помещены в металлический корпус и залиты электролитом. Разделитель (сепаратор), увлажненный электролитом, изолирует пластины друг от друга. Он изготавливается из нетканого материала, который должен быть устойчив к воздействию щелочи. Электролитом чаще всего выступает гидрооксид калия KOH с добавкой гидроксида лития LiOH, способствующего образованию никелатов лития и увеличения емкости на 20%.
$IMAGE6$
Рисунок 3 - Напряжение на аккумуляторе во время заряда или разряда, в зависимости от текущего уровня зарядки.
Во время разрядки активные никель и кадмий трансформируются в гидрооксиды Ni(OH)2 и Cd(OH)2.
К основным преимуществам Ni-Cd аккумуляторов относятся:
- низкая стоимость;
- работа в широком температурном диапазоне и устойчивость к ее перепадам (например, Ni-Cd аккумуляторы могут заряжаться при отрицательной температуре, что делает их незаменимыми при работе в условиях крайнего севера);
- они могут отдавать в нагрузку значительно больший ток, чем другие виды аккумуляторов;
- устойчивость к большим токам заряда и разряда;
- относительно короткое время заряда;
- большое количество циклов «заряда-разряда» (при правильной эксплуатации они выдерживают более 1000 циклов);
- легко восстанавливаются после длительного хранения.
Недостатки Ni-Cd аккумуляторов:
- наличие эффекта памяти — если регулярно ставить не до конца разряженный аккумулятор на зарядку, его емкость будет снижаться за счет роста кристаллов на поверхности пластин и других физико-химических процессов. Чтобы аккумулятор не «отдал концы» раньше времени, хотя бы раз в месяц его необходимо «тренировать», о чем сказано чуть ниже;
- кадмий — очень токсичное вещество, поэтому производство Ni-Cd аккумуляторов плохо сказывается на экологии. Также возникают проблемы с переработкой и утилизацией самих аккумуляторов.
- низкая удельная емкость;
- большой вес и габариты по сравнению с другими типами аккумуляторов при одинаковой емкости;
- высокий саморазряд (после заряда за первые 24 часа работы теряют до 10%, а за месяц — до 20% запасенной энергии).
$IMAGE7$
Рисунок 4 - Саморазряд Ni-Cd аккумуляторов
В настоящее время число выпускаемых Ni-Cd аккумуляторов стремительно сокращается, им на смену пришли, в частности, Ni-MH