А.В.Гордеева, Ю.А.Лабас
Альтруизм (от лат. аlter - другой) - нравственный принцип, заключающийся в бескорыстном служении другим людям, в готовности жертвовать для их блага личными интересами. Такое определение альтруизма дал французский философ Огюст Конт. “Vivre pour altrui” (жить для другого) имеет русский аналог: “Сам погибай, а товарища выручай”.
Альтруистическое поведение присуще не только людям, но и высшим животным. Обычно животные проявляют альтруизм, предупреждая собратьев об опасности. Особь, подавшая сигнал к бегству, часто привлекает к себе внимание хищника и становится его жертвой.
Оказалось, что альтруисты встречаются на всех уровнях организации живой материи, начиная с клеточного. Ради блага организма гибнут не только отдельные клетки, но и целые органы. Этот процесс мы видим всякий раз, когда наблюдаем превращение головастиков в лягушат, ловим ящериц или гуляем по осеннему лесу. Альтруизм свойствен, например, клеткам яблочной плодоножки. Ведь если бы все яблоки оставались на ветвях, как бы они размножались? Запрограммированная смерть клеток получила название “апоптоз”, что в переводе с греческого означает “листопад”.
В последние годы выяснилось, что совершают самоубийство и одноклеточные организмы. Каковы у них механизмы и назначение этого процесса? Как клетки “научились” организованно погибать “по команде” и по какой именно? Этим вопросам и посвящена наша статья. Но вначале рассмотрим, зачем, почему и каким образом совершают самоубийства клетки многоклеточных.
Зачем и почему
Для чего многоклеточному организму может понадобиться гибель отдельных его клеток? Примеры ее использования во благо целого организма мы уже приводили, когда говорили об осенних листьях и яблоках, о хвостах головастиков и ящериц. Белые кровяные клетки - макрофаги - заглатывают болезнетворных бактерий и, совершая самоубийство, убивают их вместе с собой. Образование пальцев у эмбриона происходит оттого лишь, что гибнут клетки в межпальцевых перегородках. Когда клетки соединительной ткани начинают превращаться в раковые, здоровые соседние клетки принудительно отправляют их в апоптоз.
Разумеется, не всегда запрограммированная смерть клеток приносит явную пользу. В отдельных случаях, таких как массовая гибель еще не сформировавшихся яйцеклеток в яичниках эмбрионов, ее назначение непонятно. Апоптоз клеток головного мозга при болезни Альцгеймера (старческом слабоумии) причиняет явный вред организму. Но в подавляющем большинстве случаев апоптоз ответствен за формообразовательные процессы, за избавление от клеток с измененным генетическим материалом или зараженных. Следовательно, для нормальной жизнедеятельности он действительно необходим.
Как отличить клетку-самоубийцу? Такие клетки отделяются от внеклеточного матрикса, их мембраны сморщиваются, ядра сжимаются, молекулы ДНК рвутся на мелкие кусочки и в итоге образуются так называемые апоптозные тельца - мембранные пузырьки с клеточным содержимым. Принимая роковое решение, клетка заблаговременно сама готовит себя к погребению: вызывает “ритуальных агентов”, роль которых исполняют макрофаги или соседние клетки. Один из липидов внутреннего слоя клеточной мембраны, фосфатидилсерин, переходит во внешний слой. Макрофаги постоянно выделяют особый гликопротеин MFG-E8 (milk fat globule-EGF-factor 8 - фактор роста эпидермальных клеток-8 из жировых глобул молока), который специфически связывается с фосфатидилсерином на поверхности клеток, впадающих в апоптоз. Образующиеся комплексы фосфатидилсерина с MFG-E8 и служат теми метками, по которым узнают будущих самоубийц. Макрофаги сбегаются к таким клеткам и быстро поглощают образовавшиеся апоптозные тельца.
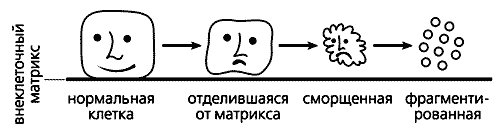
Схема, иллюстрирующая морфологические изменения клетки при апоптозе.
Есть и другой вид запрограммированной смерти, еще недавно не считавшийся таковым, - некроз. При некрозе клетка не съеживается, а, напротив, набухает; то же происходит и со всеми ее органеллами. Это приводит к нарушению целостности всех мембранных структур, в первую очередь лизосом, и, как следствие, к автолизу. Содержимое клетки вместе с активными протеолитическими ферментами изливается в межклеточное пространство, повреждая все вокруг себя. Этот процесс сопровождает воспалительные заболевания, ожоговую болезнь и т.д., иначе говоря, все случаи, когда гибельные стимулы слишком сильны для того, чтобы клетка успела достойным образом подготовиться к смерти. Такой способ самоубийства вряд ли можно считать альтруистическим, поэтому мы не будем на нем останавливаться.
Почему же клетка решает умереть? По приведенным примерам можно судить о причинах, побуждающих клетку к суициду. Убивают себя либо уже больные клетки, либо те, гибель которых в данном месте в данное время выгодна организму. Если больная клетка “не хочет” сама совершать самоубийство, ее могут побудить к этому соседи.
Не счесть орудий самоубийства
Клетка узнает, что должна покончить собой, получив “извещение о предстоящей смерти”. Роль таких извещений выполняют специальные сигнальные белки, в число которых входит и фактор некроза опухолей, выделяемый макрофагами. Приемниками сигнальных молекул служат рецепторные белки, расположенные на поверхности клеток и называемые “рецепторами смерти”. Действие этих сигналов опосредовано особыми протеолитическими ферментами (каспазами) и адаптерными белками, которые помогают им связаться с рецепторным комплексом.
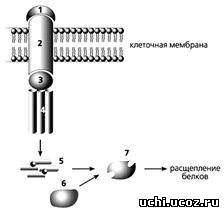
Рецепторный путь апоптоза.
Сигнальная молекула (1) связывается с “рецептором смерти” (2) и далее через адаптерный белок (3) - с прокаспазой-8 (4), после чего она превращается в активный фермент каспазу-8 (5). Она активирует в свою очередь прокаспазу-3 (6), которая, став действующим ферментом (7), расщепляет клеточные белки, и клетка погибает.
У млекопитающих семейство каспаз состоит из 14 постоянно синтезируемых белков. Неактивная каспаза, или прокаспаза, построена из четырех частей: N-концевого домена, большой и малой субъединиц и короткой связующей области между ними. Чтобы прокаспаза превратилась в активный фермент, связующая область и N-концевой домен отщепляются, и образуется гетеродимер из большой и малой субъединиц. Из двух таких димеров и формируется активная каспаза. При апоптозе сначала активируются инициаторные каспазы (-2, -8, -9, -10, -12), а затем, с их помощью, эффекторные (-3, -6, -7). Эти последние расщепляют опорно-двигательные структуры клетки, подавляют биосинтез белков и приводят в действие эндонуклеазу - фермент, расщепляющий ДНК. Остальные каспазы (-1, -4, -5, -11, -13, -14) принимают участие в развитии воспалительных процессов, а также, наряду с эффекторными каспазами, в формировании эпителиальных клеток хрусталика, кератиноцитов (клеток верхнего слоя кожи) и т.д.
После того как сигнальная молекула связалась с “рецептором смерти”, с помощью адаптерного белка к ним присоединяется прокаспаза-8. Став в результате этого работающим ферментом, она активирует прокаспазу-3, стоящую на пересечении двух путей запуска апоптоза - рецепторного и митохондриального. Роль каспазы-3 - расщепление опорных клеточных структур.
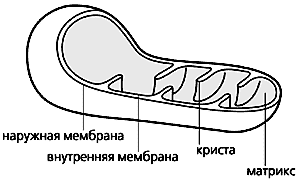
Схема строения митохондрии.
Митохондрии, эти клеточные органеллы с двойной мембраной, обладают, как известно, собственным геномом и способны автономно размножаться. Внутренняя мембрана образует глубокие складки - кристы. В ограниченном ею пространстве, митохондриальном матриксе, находятся ферменты энергетического метаболизма. Митохондрии обеспечивают всю клеточную жизнь, поскольку служат энергетическими станциями: здесь энергия питательных субстратов запасается в доступной для клетки форме, в виде аденозинтрифосфата (АТФ). Он синтезируется за счет энергии, высвобождающейся при переносе электронов с атомов водорода, образовавшихся при переработке субстратов, на конечный акцептор - кислород. Белки, переносящие электроны, встроены во внутреннюю мембрану митохондрий и образуют электронтранспортную цепь (ЭТЦ). Ее конечный элемент - цитохром с-оксидаза - и передает электроны от цитохрома с на кислород (это клеточное дыхание).
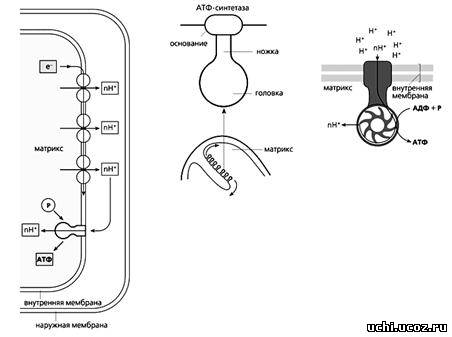
Схема окислительного фосфорилирования (слева), в ходе которого синтезируется АТФ. Высокоэнергетические электроны проходят по переносящей их цепи, и часть высвобождаемой при этом энергии используется для откачивания протонов из матрикса. На внутренней мембране возникает электрохимический протонный градиент, благодаря чему Н+ снова возвращаются в матрикс через АТФ-синтетазу. Этот фермент использует энергию протонного тока для синтеза АТФ из АДФ и неорганического фосфата (P). На рисунке приведены также схема строения АТФ-синтетазы (в середине) и модель действия этого фермента.
Протоны, оставшиеся после отрыва электронов от атомов водорода, за счет энергии электронного транспорта выталкиваются из матрикса в межмембранное пространство. Возникающая при этом разность концентраций (градиент) ионов Н+ создает мембранный потенциал митохондрий (Dym), энергия которого и используется для фосфорилирования аденозиндифосфата (АДФ).
Фермент АТФ-синтетаза, катализирующий образование АТФ из АДФ и неорганического фосфата, представляет собой встроенное во внутреннюю мембрану грибовидное тельце с каналом в центре. Когда ион Н+ прорывается по этому каналу в матрикс, энергия протонного тока идет на синтез АТФ. Других путей возвращения в матрикс у протона нет, поскольку в нормальном состоянии внутренняя мембрана непроницаема для ионов. Процесс синтеза АТФ за счет энергии переноса электронов называется окислительным фосфорилированием.
В матриксе протоны соединяются с кислородом, восстановленным в ходе работы электронтранспортной цепи, и образуется вода. Но если он восстанавливается не полностью, появляются активные формы кислорода (АФК): супероксидный радикал (О2·–), перекись водорода (Н2О2) и гидроксильный радикал (ОН·). В митохондриях образование АФК, этого побочного продукта, усиливается при повышении скорости потока электронов, увеличении концентрации кислорода и разобщении дыхания и окислительного фосфорилирования веществами, которые вызывают проницаемость внутренней мембраны.
Органеллы, обеспечивающие жизнедеятельность клетки, обеспечивают и ее смерть. При сильном стрессовом воздействии (переохлаждении; нагревании; стимуляции образования АФК другими структурами клетки, помимо митохондрий; перекисном окислении липидов плазматической мембраны - чаще всего при облучении) в цитоплазме резко повышается концентрация ионов кальция. Если кальциевые депо клетки не справляются с его утилизацией, открывается так называемая митохондриальная пора диаметром 2.6-2.9 нм. Она представляет собой канал, проходящий через обе митохондриальные мембраны и состоящий из трех белков: транслокатора адениновых нуклеотидов, потенциалзависимого анионного канала (порина) и бензодиазепинового рецептора. Когда этот комплекс связывается с Са2+, через мембранную пору могут проходить вещества с небольшой молекулярной массой. Это приводит к падению мембранного потенциала и набуханию матрикса, целостность внешней мембраны неизбежно нарушается, и из межмембранного пространства в цитоплазму выходят белки апоптоза. Их несколько: фактор, индуцирующий апоптоз (APOptosis-inducing factor - AIF), вторичный митохондриальный активатор каспаз (second mitochondria-derived activator of caspases - Smac) и некоторые прокаспазы. Индуцирующий фактор направляется прямо в ядро, где вызывает деградацию ДНК.
Наряду со специфически апоптозными белками, из митохондрии через открытую пору выходит цитохром с, который в норме служит конечным звеном электронтранспортной цепи. В цитоплазме этот белок связывается с белком Apaf-1 (APOptotic protease activating factor-1 - активирующий протеазу фактор-1) и формирует апоптосомный комплекс. Он с помощью Smac и еще одного фактора (Omi/HtrA2) активирует прокаспазу-9, та, став каспазой-9, превращает два других профермента в каспазы-3 и -7; а они уже расщепляют структурные белки, приводя к появлению биохимических и морфологических признаков апоптоза. В числе первых можно назвать, в частности, переход фосфатидилсерина в наружный мембранный слой и фрагментацию ДНК. Из вторых признаков наиболее характерны “отшелушивание” клетки от матрикса, сморщивание мембраны, сжатие ядра и формирование пузырьков с клеточным содержимым - апоптозных телец.
Цитохром с электростатически и гидрофобно связан с внутренней мембраной митохондрий через фосфолипиды, преимущественно через кардиолипин. Электростатически взаимодействуют между собой положительно заряженные остатки аминокислоты лизина в цитохроме и отрицательно заряженные фосфатные группы в кардиолипине. За счет гидрофобного взаимодействия между углеродной цепью этого фосфолипида и гидрофобными участками молекулы цитохрома еще более укрепляется связь фермента с митохондриальной мембраной, что обеспечивает даже его частичное погружение в ее слой.
Следовательно, для выхода цитохрома с в цитоплазму одного лишь нарушения целостности митохондриальной мембраны недостаточно. Электростатически связанный цитохром с может оторваться от кардиолипина, если изменяется ионная сила, плотность поверхностного заряда или рН, а связанный гидрофобно - за счет окислительной модификации митохондриальных липидов. Последнюю реакцию как раз и вызывают активные формы кислорода, которые неизбежно образуются при любых сильных воздействиях (стрессах), а открывание поры усиливает этот процесс.
Однако цитохром с не всегда нужен для запрограммированной смерти. Апоптоз в сердечной ткани, например, вообще протекает без этого фермента, он так и не выходит из межмембранного пространства.
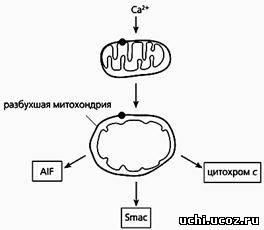
Фрагмент схемы апоптоза, протекающего по митохондриальному пути.
Под действием избытка ионов кальция митохондрия разбухает, через пору из нее выходит цитохром с и два белка - AIF и Smac. Первый белок индуцирует апоптоз, а второй активирует некоторые прокаспазы.
Цитохром с может высвобождаться в ответ на повышение концентрации